Herzinsuffizienz – Das schwache Herz
Rund vier Millionen Menschen in Deutschland leiden an Herzinsuffizienz.1 Bei der Klassifikation einer Herzinsuffizienz unterscheidet man nach dem Ort des Auftretens z.B. in Linksherzinsuffizienz, Rechtsherzinsuffizienz oder globale Herzinsuffizienz. Auch der zeitliche Verlauf ist ein wichtiges Kriterium. Tritt eine Herzinsuffizienz nach einem akuten Ereignis, z.B. einem Herzinfarkt oder nach schweren Herzrhythmusstörungen auf, wird sie als akut bezeichnet. In diesem Fall ist eine sofortige Einweisung ins Krankenhaus erforderlich.
Im besten Fall kann der Auslöser der Herzinsuffizienz therapiert werden, zudem finden auch Begleiterkrankungen Berücksichtigung, um eine ganzheitliche Behandlung zu ermöglichen. Die Therapiemaßnahmen bei einer chronischen Herzinsuffizienz zielen darauf ab, das Fortschreiten der Erkrankung zu hemmen, die Symptome zu mildern sowie die körperliche Belastungsfähigkeit, Lebensqualität und Prognose der Patient:innen zu verbessern. 2
Welche therapeutische Maßnahme wann für Patient:innen infrage kommt, ist abhängig vom jeweiligen Krankheitsstadium und wird gemeinsam mit dem medizinischen Personal festgelegt. Neben dem Einsatz von Medikamenten, beispielsweise zur Regulation des Bluthochdruckes oder Verdünnung des Blutes, stellt die Implantation von medizintechnischen Geräten eine Option dar.
Stadien der Herzinsuffizienz
Da sich die chronische Herzinsuffizienz über einen längeren Zeitraum entwickelt, wird sie mit Hilfe der New York Heart Association (NYHA)-Klassifikation in vier Stadien eingeteilt. 2
Häufige Symptome einer Herzinsuffizienz
Häufige Symptome eine Herzinsuffizienz sind:
Wichtig zu wissen:
Suchen Sie schon bei ersten Symptomen einer Herzinsuffizienz sofort medizinische Hilfe. In der kardiologischen Praxis wird ein EKG, Ultraschall des Herzens, Blutuntersuchung, Blutdruckmessung oder Belastungstests gemacht und die Krankheitsgeschichte abgefragt, um Kenntnis über Herzinsuffizienz verursachenden Erkrankungen (Bluthochdruck, Klappenerkrankungen, koronare Herzkrankheiten) zu bekommen.16 Auch Begleiterkrankungen und risikobeeinflussende Lebensstilfaktoren (z.B. Rauchen, körperliche Inaktivität) werden überprüft.
Reduzierte Belastbarkeit als Folge des Sauerstoffmangels
Bei allen Formen der Herzinsuffizienz ist das Herz nicht mehr in der Lage, den Organismus ausreichend mit Blut und Sauerstoff zu versorgen, um einen stabilen Stoffwechsel unter Ruhe- und Belastungsbedingungen zu gewährleisten.16 Ursächlich für die reduzierte Pumpleistung des Herzens oder die Schwäche des Herzmuskels ist in den meisten Fällen eine Vorerkrankung. Muss das Herz beispielsweise gegen einen höheren Widerstand – wie bei Bluthochdruck – arbeiten, vergrößert sich der Herzmuskel und wird dadurch schwächer. In rund zwei Drittel der Fälle beruht die Herzschwäche auf einer koronaren Herzkrankheit.2 Auch ein Herzinfarkt oder eine durch einen Infekt ausgelöste Entzündung kann den Herzmuskel derart schädigen, dass die Funktion stark eingeschränkt ist.
In epidemiologischen Untersuchungen erwiesen sich auch Diabetes, Rauchen, starker Alkoholkonsum, körperliche Inaktivität, Adipositas, eine familiäre Veranlagung für Kardiomyopathien sowie bestimmte Arzneimittel und Therapieverfahren für die Behandlung von Tumorerkrankungen als risikoerhöhend.16 Ein häufiger Auslöser einer Herzinsuffizienz ist eine Herzklappenerkrankung, wie etwa die Mitralklappeninsuffizienz.
Wichtig zu wissen:
Die Prävention der chronischen Herzinsuffizienz basiert im Wesentlichen darauf, Patient:innen mit einem erhöhten Risiko, z.B. für Diabetes mellitus Typ 2 oder eine koronare Herzkrankheit, frühzeitig zu identifizieren und entsprechend zu therapieren.
Herzschwäche durch Mitralklappeninsuffizienz
Die Mitralklappeninsuffizienz oder auch kurz Mitralinsuffizienz (MI) ist eine der häufigsten Herzklappenerkrankungen in Europa. Etwa 1 von 10 Menschen über 75 Jahren leidet unter einer mäßigen bis schweren Mitralinsuffizienz3, das bedeutet, die Mitralklappe schließt nicht vollständig. Je nach Schweregrad fließt eine geringe bis größere Menge des mit Sauerstoff angereicherten Blutes, das eigentlich für die Organe (Gehirn, Nieren, Darm etc.) bestimmt ist, zurück in den Vorhof statt in den Körperkreislauf. Die Folgen: Um die für die Organe fehlende Menge an Blut ausgleichen zu können, pumpt der Herzmuskel vermehrt, die erhöhte Pumpleistung erwirkt eine Vergrößerung des Herzens und schwächt es auf Dauer. Dies führt zu einer Einschränkung der Belastbarkeit, Luftnot bei Anstrengung, Rückstau des Blutes im Lungenkreislauf mit der Gefahr eines Lungenödems. Letzteres ist unbehandelt lebensbedrohlich. Durch das in den Vorhof zurückfließende Blut kommt es auch zu einer Vergrößerung des Vorhofs. Das kann zu Herzrhythmusstörungen oder sogar zum Schlaganfall führen.
 Die Tendyne™ Klappe von Abbott ist die erste Behandlungsmöglichkeit ihrer Art, um die Mitralklappe von Patient:innen ohne Eingriff am offenen Herzen zu ersetzen. Während des Eingriffs wird der/die zu Operierende zunächst in Vollnarkose versetzt und im Anschluss ein Katheter über einen Schnitt auf der linken Seite des Brustkorbs bis ins Herz vorgebracht. Mithilfe dieses Katheters positioniert der/die Mediziner:in das Tendyne™ System im Herzen, wo es die Funktion der Mitralklappe übernimmt. Ein an der Klappe befestigtes Halteband – der sogenannte Tether – wird dann mit einem kleinen Pad am unteren Ende des Herzens verbunden. So bleibt die Klappe dauerhaft in ihrer Position.
Die Tendyne™ Klappe von Abbott ist die erste Behandlungsmöglichkeit ihrer Art, um die Mitralklappe von Patient:innen ohne Eingriff am offenen Herzen zu ersetzen. Während des Eingriffs wird der/die zu Operierende zunächst in Vollnarkose versetzt und im Anschluss ein Katheter über einen Schnitt auf der linken Seite des Brustkorbs bis ins Herz vorgebracht. Mithilfe dieses Katheters positioniert der/die Mediziner:in das Tendyne™ System im Herzen, wo es die Funktion der Mitralklappe übernimmt. Ein an der Klappe befestigtes Halteband – der sogenannte Tether – wird dann mit einem kleinen Pad am unteren Ende des Herzens verbunden. So bleibt die Klappe dauerhaft in ihrer Position.
Der größte Vorteil von Tendyne™ ist, dass der Eingriff viel schonender ist. Im Anschluss an den Eingriff müssen die frisch Operierten wenige Tage zur Beobachtung im Krankenhaus bleiben. Viele Opertierte berichten nach der Implantation von einer deutlichen Verbesserung ihrer Beschwerden und Steigerung der Lebensqualität.
Tipp: Eventuell verschriebene Medikamente wie beispielsweise Blutverdünner sollten auch nach dem Eingriff exakt nach den Anweisungen medizinischen Fachpersonal eingenommen werden.
Herzklappendefekt: TriClip™ ermöglicht eine minimalinvasive Herzklappenreparatur
 TriClip™ bietet Patient:innen mit einem Herzklappendefekt – genauer gesagt einem Schaden an der Trikuspidalklappe –alle Vorteile einer minimalinvasiven Operation. Hierbei wird beim Implantieren des TriClipsTM ein neues, lenkbares Führungskatheter-System verwendet. Dieses passt sich an die rechte Seite des Herzens – wo sich die Trikuspidalklappe befindet – an und ermöglicht dem/der Mediziner:in die Segel effektiv zu greifen und zu adaptieren. Durch diesen Ansatz ist das Herz in der Lage, das Blut wieder effizienter zu pumpen. Um unterschiedlichen Patient:innenanatomien gerecht zu werden, gibt es TriClipTM in zwei verschiedenen Größen.
TriClip™ bietet Patient:innen mit einem Herzklappendefekt – genauer gesagt einem Schaden an der Trikuspidalklappe –alle Vorteile einer minimalinvasiven Operation. Hierbei wird beim Implantieren des TriClipsTM ein neues, lenkbares Führungskatheter-System verwendet. Dieses passt sich an die rechte Seite des Herzens – wo sich die Trikuspidalklappe befindet – an und ermöglicht dem/der Mediziner:in die Segel effektiv zu greifen und zu adaptieren. Durch diesen Ansatz ist das Herz in der Lage, das Blut wieder effizienter zu pumpen. Um unterschiedlichen Patient:innenanatomien gerecht zu werden, gibt es TriClipTM in zwei verschiedenen Größen.
Abbotts TriClipTM kann bei der Behandlung von Menschen, die an einer schweren Trikuspidalklappeninsuffizienz (TI) leiden, wegweisend sein und diese grundlegend beeinflussen. Die TRILUMINATETM-Zulassungsstudie zeigt, dass TriClipTM den Schweregrad der TI reduziert und mit einer deutlichen Verbesserung der funktionellen Kapazität und der Lebensqualität nach zwölf Monaten einhergeht.
Elektrische Implantate
Bei einer Herzinsuffizienz können die vier Herzkammern nicht mehr synchron, d.h. im Takt schlagen. Um dies zu beheben ist die kardiale Resynchronisationstherapie (CRT) eine Behandlungsoption. Es gibt hier zwei verschiedene spezielle Implantate, die das Herz dabei unterstützen, wieder im Takt zu schlagen und so die Pumpfunktion zu verbessern: einen speziellen Herzschrittmacher und einen implantierbaren Kardioverter Defibrillator, der im Falle eines Falles auch einen lebensrettenden Schock abgeben kann.
Implantation CRT- Herzschrittmacher
 Haben Patient:innen einen sogenannten Linksschenkelblock entwickelt, was eine Störung der elektrischen Impulse im Herzen zur Folge hat, sind oft die Herzkammern vergrößert. Die linke Herzkammer pumpt dadurch nicht mehr im Takt, wodurch sich die Herzleistung zusätzlich verringert. Dieser spezielle Herzschrittmacher, sorgt über elektrische Impulse dafür, dass der linke und der rechte Ventrikel (die beiden unteren Herzkammern) zusammenarbeiten. Dadurch kann das Herz das Blut effektiver durch den gesamten Körper pumpen, was sich wiederum positiv auf die körperliche Belastbarkeit und die Lebensqualität auswirken kann.
Haben Patient:innen einen sogenannten Linksschenkelblock entwickelt, was eine Störung der elektrischen Impulse im Herzen zur Folge hat, sind oft die Herzkammern vergrößert. Die linke Herzkammer pumpt dadurch nicht mehr im Takt, wodurch sich die Herzleistung zusätzlich verringert. Dieser spezielle Herzschrittmacher, sorgt über elektrische Impulse dafür, dass der linke und der rechte Ventrikel (die beiden unteren Herzkammern) zusammenarbeiten. Dadurch kann das Herz das Blut effektiver durch den gesamten Körper pumpen, was sich wiederum positiv auf die körperliche Belastbarkeit und die Lebensqualität auswirken kann.
Im Rahmen des Eingriffs wird die Haut an der linken Brustseite unter dem Schlüsselbein durch einen kleinen Schnitt eröffnet und der Herzschrittmacher eingesetzt. Meist schließen die Spezialisten drei Elektroden das Gerät an: Hierbei handelt es sich um dünne, isolierte Drähte, die sich über eine Vene in der Nähe des Schlüsselbeins bis in den rechten Vorhof und die rechte Herzkammer vorschieben lassen. Die linke Herzkammer wird über eine Herzkranzvene an der Außenseite des Herzens stimuliert. Dazu schiebt der/die Kardiolog:in die Elektrode bis in die Herzkranzvene und platziert sie dort. Sind die Elektroden richtig positioniert, verbindet der/die Operateur:in diese mit dem Implantat und testet, ob das System korrekt funktioniert. Im Anschluss wird die Hauttasche mit einer Naht verschlossen. Patient:innen können nach kurzer Zeit das Krankenhaus wieder verlassen.
Implantation CRT-Defibrillator
Ein CRT-Defibrillator ist eine Kombination aus der kardialen Resynchronisationstherapie (CRT) und einem Elektroschockgerät, dem sogenannten implantierbaren Kardioverter-Defibrillator (ICD). Dabei werden die Vorteile der beiden implantierbaren Therapiesysteme verbunden: Das CRT-Gerät synchronisiert und stabilisiert die Arbeit der beiden unteren Herzkammern. Das Elektroschockgerät (Defibrillator) kontrolliert den Herzrhythmus und reagiert bei gefährlichen Rhythmusstörungen sofort, indem es einen lebensrettenden Schock abgibt. Dadurch kann in vielen Fällen ein plötzlicher Herztod verhindert werden. Im Rahmen des Eingriffs wird die Haut an der linken Brustseite unter dem Schlüsselbein durch einen kleinen Schnitt eröffnet und das System eingesetzt. Meist schließen die Spezialisten drei Elektroden an das Implantat an: Hierbei handelt es sich um dünne, isolierte Drähte, die sich über eine Vene in der Nähe des Schlüsselbeins bis in den rechten Vorhof und die rechte Herzkammer vorschieben lassen. Die linke Herzkammer wird über eine Herzkranzvene an der Außenseite des Herzens stimuliert. Sind die Elektroden richtig positioniert, verbindet der/die Operateur:in diese mit dem Implantat und testet, ob das System korrekt funktioniert. Im Anschluss wird die Hauttasche mit einer Naht verschlossen. Patient:innen können nach kurzer Zeit das Krankenhaus wieder verlassen.
Vorteile des CRT-D GALLANTTM HF von Abbott:
 Beim CRT-D Gallant™ HF von Abbott handelt es sich um ein implantierbares Therapiesystem, das den heutigen Anforderungen der technischen Entwicklung gerecht wird. So verfügt das System etwa über integrierte Smartphone-Konnektivität, die eine kontinuierliche Einbeziehung der Patient:innen per Telemedizin ermöglicht, sodass sich Probleme früher erkennen und behandeln lassen.
Beim CRT-D Gallant™ HF von Abbott handelt es sich um ein implantierbares Therapiesystem, das den heutigen Anforderungen der technischen Entwicklung gerecht wird. So verfügt das System etwa über integrierte Smartphone-Konnektivität, die eine kontinuierliche Einbeziehung der Patient:innen per Telemedizin ermöglicht, sodass sich Probleme früher erkennen und behandeln lassen.
Hierzu informiert die von den Patient:innen heruntergeladene „myMerlinPulse“-App die behandelnde Klinik täglich über den aktuellen Status. Doch auch über die Datenübermittlung hinaus bietet die App zahlreiche Möglichkeiten. So können Patient:innen den Batterieladestand des Implantats prüfen, bereits stattgefundene Datenübertragungen aufrufen und auf Unterstützung bei der Funktionsweise zugreifen. Auf diese Weise werden Nutzer:innen kontinuierlich in die Therapie eingebunden, was zu einer größeren Bereitschaft beim aktiven Mitwirken an therapeutischen Maßnahmen und einer erhöhten Lebensqualität beitragen kann.
Herzpumpe oder Left-Ventricular Assist Device (LVAD) HeartMate 3™
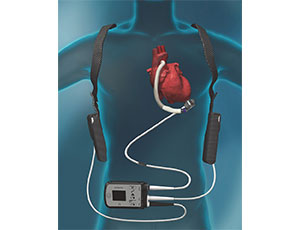 Bei Erreichen des NYHA IV-Stadiums benötigt der/die Betroffene eine Herztransplantation, da das Herz den Körper nicht mehr mit Blut versorgen kann und der Patient bettlägerig ist. Eine klinisch erprobte Alternative einer Herztransplantation, die auch die Lebensqualität des jeweiligen Menschen erheblich steigert, ist die Implantation eines sogenannten Left Ventricular Assist Device (LVAD). Dies ist eine mechanische Pumpe, wie Abbotts HeartMate 3™, die während der Operation implantiert und mit dem Herzen des Patienten verbunden wird.
Bei Erreichen des NYHA IV-Stadiums benötigt der/die Betroffene eine Herztransplantation, da das Herz den Körper nicht mehr mit Blut versorgen kann und der Patient bettlägerig ist. Eine klinisch erprobte Alternative einer Herztransplantation, die auch die Lebensqualität des jeweiligen Menschen erheblich steigert, ist die Implantation eines sogenannten Left Ventricular Assist Device (LVAD). Dies ist eine mechanische Pumpe, wie Abbotts HeartMate 3™, die während der Operation implantiert und mit dem Herzen des Patienten verbunden wird.
Ein LVAD sollte jedoch nicht mit einem Kunstherz verwechselt werden. Während letzteres ein zu schwach gewordenes Herz komplett ersetzt, hilft ein LVAD dem Herzen, mit weniger Kraftaufwand mehr Blut zu pumpen. Das System zieht dafür kontinuierlich Blut aus der linken Herzkammer und transportiert es zur Hauptschlagader, die das sauerstoffreiche Blut transportiert und dann durch den Körper strömt. Früher waren LVADs für Patienten gedacht, die eine Kurzzeittherapie benötigen, um die Wartezeit bis zu einer Herztransplantation zu überbrücken. Sie können aber inzwischen aber auch zur Langzeittherapie eingesetzt werden, wenn das Herz noch viele Jahre unterstützt werden muss, weil für die Patient:in eine Herztransplantation in Frage kommt oder der/die Bertroffene keine Transplantation wünscht.
Die Rolle von Menschen mit Typ-F bei der Rehabilitation
Während der Genesungszeit empfiehlt das medizinisches Fachpersonal dem frischoperierten Menschen eventuell für eine gewisse Zeit körperliche Anstrengungen einzuschränken, aber nach einer Phase der Heilung können die meisten Personen in der Regel wieder ihre vor der Implantation gewohnten Aktivitäten ausüben. Idealerweise lernen die Patient:innen in einer stationären oder ambulanten Rehabilitation bereits viel über einen herzgesunden Lebensstil, den Abbau von Stressfaktoren und auch dem Umgang mit psychischen Problemen, die eine Herzerkrankung auslösen bzw. verstärken können. Im Umgang mit dieser seelischen Belastung können Sie als Mensch mit Typ F im Alltag ebenso eine große Hilfe sein, wie auch – ganz praktisch – bei der Einhaltung von Nachsorgeterminen. Auch die Umsetzung einer genussvollen, herzgesunden Ernährung, die Integration von Bewegung und das Finden einer guten Work-Life-Balance gelingt zusammen besser als allein.
Was man nach einer Implantation beachten sollte:
Nach der Implantation eines medizintechnischen Systems kann man wieder aktiv sein, bedenkenlos reisen, die meisten Maschinen bedienen, Mobiltelefone verwenden und Auto fahren. Wichtig ist lediglich Stöße oder Prellungen zu vermeiden. So könnten beispielsweise bei Kontaktsportarten Teile des Systems beschädigt werden. Patien:innen mit einer HeartMate 3 Herzpumpe sollten Baden, Schwimmen und Saunieren meiden. Besprechen Sie zusammen mit Ihrem/Ihrer herzkranken Angehörigen oder Freund:in welches Hobby oder Sportprogramm er/sie wieder aufnehmen möchte und klären Sie Fragen mit dem Team der behandelnden kardiologischen Praxis ab.5
Quellen
1 Deutsche Herzstiftung e.V., Herzschwäche: Symptome und Therapie, online verfügbar unter https://www.herzstiftung.de/infos-zu-herzerkrankungen/herzinsuffizienz
2 Bundesärztekammer (BÄK), Kassenärztliche Bundesvereinigung (KBV), Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF). Nationale Versorgungsleitlinie Chronische Herzinsuffizienz – Langfassung, 3. Auflage. Version 3. 2019 [cited: YYYY-MM-DD]. DOI: 10.6101/AZQ/000482. www.leitlinien.de/herzinsuffizienz.
3 Nkomo VT, Gardin JM, Skelton TN, Gottdiener JS, Scott CG, Enriquez-
Sarano M, Burden of valvular heart diseases: a population-based study.
Lancet 2006j 368 (9540):1005-1011
4 Cio G, Tarantini L, De Feo S et al. Functional mitral regurgitation predicts
1-year mortality in elderly patients with systolic chronic heart failure. Eur J
Heart Fail. 2005; 7(7):1112-1117
5 Was erwartet mich bei meinem CRT-Gerät, Patientenbroschüre Abbott, © 2020 Abbott. Alle Rechte vorbehalten. 37652 MAT-2001907 v1.0 | Dieses Dokument
Links, die Sie von den weltweiten Abbott-Websites zu anderen Seiten leiten, unterliegen nicht der Kontrolle durch Abbott und Abbott ist nicht für die Inhalte einer solchen Website oder untergeordnete Links solcher Websites verantwortlich. Abbott stellt diese Links nur als weiterführende Informationen zur Verfügung, und die Einbeziehung eines Links bedeutet nicht, dass Abbott die verlinkte Seite billigt.
Die Website, die Sie angefordert haben, ist vielleicht nicht für Ihre Bildschirmgröße optimiert.